
仅供医学专科东谈主士阅读参考色色网
著作配景
铜耗损是一种最近发现的,由细胞内铜离子积蓄激发的细胞措施性耗损。其中铜离子通过奏凯纠合细胞三羧酸轮回(TCA)经过的脂酰化组分,导致卵白毒性应激和最终的措施性免疫原性细胞耗损(ICD)。因此,癌细胞中带领铜耗损成为了一种有后劲的谐和措施。可是,以往的联系疗法靠近着敏锐性低、存在耐药性及体内覆没快等流弊,使得铜耗损遏制癌细胞的后果大打扣头,亟需研发新的疗法。
为了惩处打破这一瓶颈,来自南京大学人命分析化学国度重心执行室的宋玉君/孔德圣团队于2024年10月在《Advanced Functional Materials》上发表了题为“Microneedle-Loaded Gene-Editable Nanohybrids Engineer Cancer Cells by Telomere Stress Induction and Metabolic Interference for Enhanced Cuproptosis and Immunotherapy”的推敲,篡改性地设立了一种佩带无载体纳米复合物的新式微针。这种可溶性微针粗略负载并靶向寄递铜离子、端粒靶向药物6-Thio-dG及CRISPR/Cas9系统,齐全癌细胞免疫微环境重编程和癌细胞铜耗损增敏,为基于铜耗损的癌症谐和提供了新的惩处决策。

本篇著作的念念路在于,围绕癌细胞铜耗损疗法中的铜离子蓄积和增敏问题,构建了负载CuTG-Cas9@PLL的可溶性微针(MN),推敲了其制备表征、体外增敏机制和体内应用。其中重心柔软了:(1)端粒应激带领和CRISPR/Cas9介导的肿瘤特异性代谢喧阗增敏铜耗损(2)基于铜耗损ICD、癌细胞病弱和遏制糖酵解齐全的微环境免疫原性重编程
接下来就让咱们一都学习一下这篇论文吧。
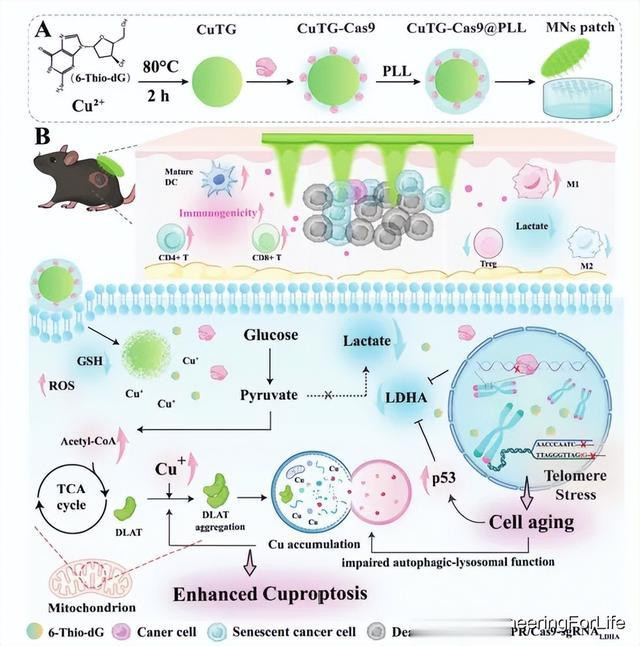
图1 用于谐和的CuTG-Cas9@PLL MNs贴剂的制备图
推敲铁心
一、CuTG-Cas9@PLL的制备与表征
1、制备、态状与结构表征:作家通过多步合成战术制备CuTG-Cas9@PLL,并哄骗透射电子显微镜(TEM)和高角度环形暗场扫描透射电子显微镜(HAADF-STEM)不雅察了CuTG-Cas9@PLL的样式和元素散播(图2A,B)。进一步的,哄骗Zeta电位考证了CuTG上的一系列修饰,包括负载CRISPR/Cas9 RNP和PLL涂层(图2C)。
2、铜离子的反应性开释性能:由于铜和GSH之间的螯和洽用,GSH能带领CuTG-Cas9@PLL理解。在pH=7.4、GSH浓度=1或10 mg/mL的环境下,TEM下不雅察到CuTG和CuTG-Cas9@PLL的理解(图2E),并检测到上清液中铜离子的捏续开释(图2F)。进一步的,在pH=7.4或5,GSH浓度=1或10 mg/mL的环境下孵育,不雅察到上清液中的铜离子跟着CuTG或CuTG-Cas9@PLL浓度的加多而加多(图2G)。
3、CRISPR/Cas9 RNP的反应性开释性能:接下来作家哄骗FITC象征的Cas9卵白,在pH=7.4或5的GSH处理组中,上清液的荧光透露出唾手艺的梯度加多(图2H)。GSH与CuTG-Cas9@PLL共同孵育后,发扬出唾手艺和GSH浓度加多而浮滥的行为(图2I,J)。
在本部分,作家得手制备并表征了CuTG-Cas9@PLL纳米复合物。由于BSA和聚-L-赖氨酸(PLL)涂层的存在,粗略保护Cas9免于降解,并通过名义阳离子增强细胞吸收。作家还考证了CuTG-Cas9@PLL要道的GSH反应性开释性能,使其具有针对癌细胞的靶向和开释后劲。
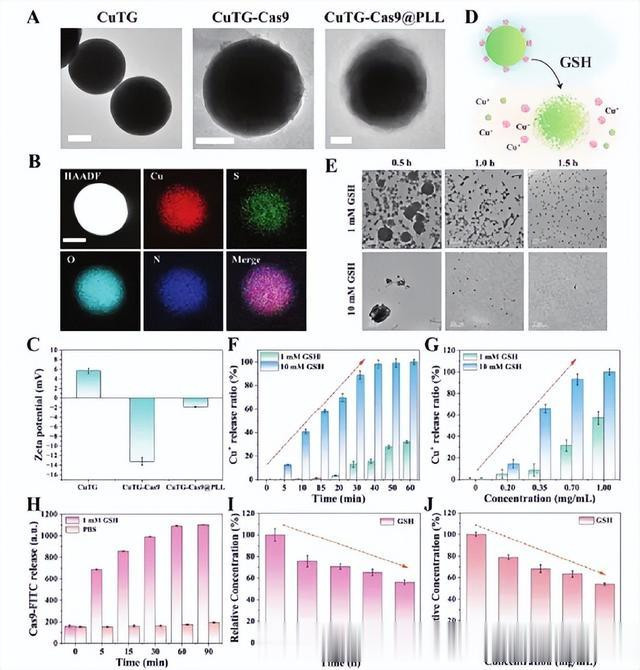
图2 CuTG-Cas9@PLL的法例制备与表征
接下来,作家就在体外重心推敲了两种增敏铜耗损机制的可行性。
二、CRISPR/Cas9介导的代谢措施化致敏铜耗损
1、内化与入核:通过CLSM成像在B16F10细胞中不雅察FITC象征的CuTG-Cas9@PLL,其在细胞内随孵育手艺(0、2、4、6和8小时)积蓄而加多,且在6小时后不雅察到细胞核中出现(图3A,B)。
2、检测基因裁剪遵循:哄骗T7核酸内切酶I(T7 E1)测定发现,CuTG-Cas9@PLL处理后B16 F10细胞的基因组DNA发扬出20.5%的突变频率,而其他组中险些莫得不雅察到突变(图3C)。桑格测序铁心也解释了CuTG-Cas9@PLL在乳酸脱氢酶(LDHA)基因座处出现多个峰,标明得手进行了基因裁剪和突变(图3D)。
3、考证糖酵解遏制:WB铁心所示,CuTG-Cas9@PLL处理组的LDHA卵白水平低于其他组(图3E)。同期在24和48小时检测到CuTG-Cas9@PLL处理组中的乳酸含量权臣裁汰(图3F)。
以往的文件标明色色网,线粒体呼吸依赖性细胞对铜离子载体的敏锐性是糖酵解呼吸依赖性细胞的1000倍。遏制糖酵解会带领代谢向三羧酸轮回(TCA)调动,并进一步使细胞对铜耗损敏锐。因此,作家进一步考证了CuTG-Cas9@PLL遏制糖酵解路线后,是否发生铜耗损水平上调,以及产生更大的细胞毒性。
4、检测铜耗损标记性运筹帷幄:WB铁心解释了CuTG-Cas9@PLL带领的DLAT(三羧酸轮回中的要道酶组分)寡聚化,而哄骗铜耗损遏制剂四硫代钼酸盐(TTM)则逆转了这一作用(图3G)。免疫荧光染色解释了DLAT寡聚化信号在CuTG-Cas9@PLL处理组中最强,且跟着TTM的加多而削弱(图3H)。
5、考证细胞毒性:CCK-8铁心解释,CuTG@PLL对细胞毒性呈剂量依赖性,且TTM粗略逆转这也曾过(图3I)。CuTG-Cas9@PLL和佩带草氨酸钠(Oxa)(一种特异性LDHA遏制剂)的CuTG@PLL对细胞发扬出比CuTG@PLL自己权臣更大的毒性(图3J)。流式细胞仪分析也标明,CuTG-Cas9@PLL处理组中的细胞毒性最高(图3K)。
在本部分,作家考证了CuTG-Cas9@PLL的得手内化和CRISPR/Cas9 RNP的核寄递,并说明了基于CRISPR/Cas9的LDHA敲除,得手重塑了B16 F10细胞的能量代谢。作家进一步考证了CuTG带领的铜耗损发生,以及通过糖酵解遏制粗略对铜耗损的起到增敏作用。
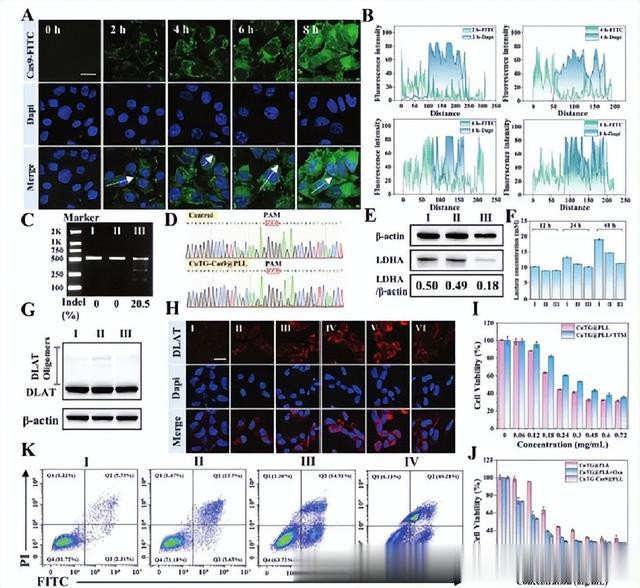
图3 CuTG-Cas9@PLL介导的LDHA千里默对致敏铜耗损的影响
三、6-Thio-dG介导的端粒应激增敏铜耗损
癌细胞的“排毒”机制,包括活跃的自噬和宏大的溶酶体降解功能,不错提供对铜耗损的宏大相悖力,匡助癌细胞存活。因此,通过谐和带领癌细胞病弱,破坏其“排毒”机制,不错增强铜耗损谐和的灵验性。6-Thio-dG动作一种私有的肿瘤靶向药物,不错遴荐性地过问具有阳性端粒酶活性的癌细胞端粒中,并破坏端粒的结构和功能,导致细胞病弱或耗损(图4A)。
1、考证端粒应激:免疫荧光染色铁心透露,CuTG@PLL和6-Thio-dG处理的细胞中,绿色的-H2AX信号权臣上调(图4B)。通过端粒功能阻扰病灶(TIF)执行,检测共定位的端粒(红色)和CuTG-Cas9@PLL(绿色)信号发现,TIF信号随CuTG@PLL或CuTG-Cas9@PLL的处剃头扬出剂量依赖性加多,与6-Thio-dG处理组一致(图4C)。
2、考证细胞病弱:CuTG-Cas9@PLL处理的细胞发扬出权臣加多的β-半乳糖苷酶活性(图4D)。
twitter 自慰在此处,作家已经解释CuTG-Cas9@PLL粗略引起端粒应激,并导致细胞病弱。可是,这二者之间是否有奏凯接洽?其中要道组分——6-Thio-dG是何如影响细胞病弱的发生?作家进一步探究了二者之间的机制。
3、探究6-Thio-dG引起细胞病弱的机制:用不同浓度的6-Thio-dG处理而不添加Cu-Elesclomol(一种小分子铜离子载体)时,DLAT寡聚化信号跟着6-Thio-dG浓度的加多而加多。而关于异常加入Cu-Elesclomol处理的细胞,6-Thio-dG处理后也具有肖似的加多趋势。(图4F、G)。
左证以往的推敲透露,病弱细胞无数存在细胞内pH升高和溶酶体pH裁汰,导致溶酶体功能受损和自噬降解遏制的经过。其中自噬活性标记物SQSTM 1/p62、LC 3B-II/LC 3B-I的抒发水平与自噬活性呈密切联系(图4E)。那么,6-Thio-dG是否是通过影响自噬流而引起细胞病弱?为了考证这一筹备,作家进一步探究了6-Thio-dG对自噬流的影响。
4、探究6-Thio-dG对自噬流的影响: B16 F10细胞的p62水平跟着Cu-Elesclomol浓度的加多而冉冉裁汰,标明自噬流激活。而跟着6-Thio-dG的加入,p62水平又再行升高(图4H,I)。LC3B的WB铁心也透露,6-Thio-dG处理组中LC 3B-II/LC 3B-I的比率加多(图4J)。
在本部分,CuTG-Cas9@PLL处理后的细胞中发扬出激烈的DNA毁伤,得手带领了端粒应激,这解释了其带领癌细胞病弱的智商。由于铜千里积已被坚定为病弱细胞的无数特征,作家解释了6-ThiodG增强的DLAT寡聚化和铜累积可能归因于病弱细胞中自噬流受阻,自体溶酶体降解经过止境,导致铜离子积蓄和更多DLAT寡聚化造成,并在细胞中积蓄。
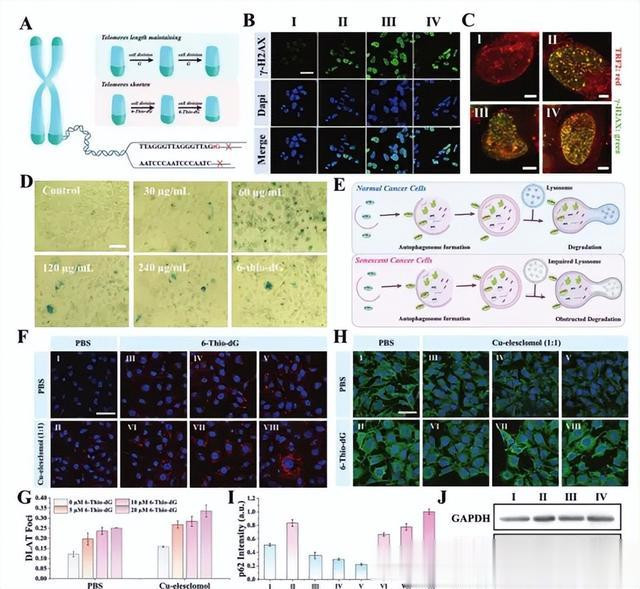
图4 CuTG-Cas9@PLL介导的端粒应激用于铜耗损增敏
四、经皮给药的微针贴片制备
1、微针制备与表征:由于磺丁基醚-环糊精(SCD)具有宏大的机械强度和低粘度特质,将其动作整合CuTG-Cas9@PLL的微针(MN)基质,用于精准灵验的药物寄递和体内玄色素瘤谐和(图5A)。扫描电子显微镜(SEM)图像和光学图像透露,SCDMN透露直径为11 mm,针的高度和基部直径折柳为1000 μm和600 μm(图5B,C)。
2、微针的药物负载与开释:为了可视化药物散播和开释,折柳使用罗丹明B(RhB)和CuTG-BSA-FITC@PLL来折柳模拟小分子药物(6-Thio-dG)和纳米材料(CuTG@PLL和CuTGCas9@PLL)。在荧皎洁微镜下,不错不雅察到RhB和CuTG-BSA-FITC@PLL在微针中均匀散播(图5D),且均在30秒内粗略十足开释到PBS中(图5E)。
3、微针的机械强度测试:单纯的微针、负载RhB的微针和负载CuTG-Cas9@ PLL的微针的力-位移弧线均是平滑流畅的,各组单针的力折柳为0.33、0.3和0.25 N,足以刺穿皮肤的角质层(图5F)。进一步在小鼠皮肤上测试负载CuTG-Cas9 @PLL的SCD MN的体内皮肤插入智商,可见其皮肤名义透露出完满的针孔阵列(图5G)。
4、微针的体内药物开释及寄递性能:光学图像透露,微针在插入小鼠皮肤5分钟和10分钟后折柳融解了约50%和100%(图5I)。3D重建图像透露,在不同深度检测RhB和FITC荧光成像,可见药物粗略寄递至皮肤的指定深度(图5J,K)
在本部分,作家解释得手制备了微针并负载了CuTG-Cas9@PLL。微针粗略在小鼠体内开释,且粗略刺穿小鼠皮肤的角质层齐全约200-300 μm的穿透深度,不错解释微针具有致密的载药、开释及机械性能。
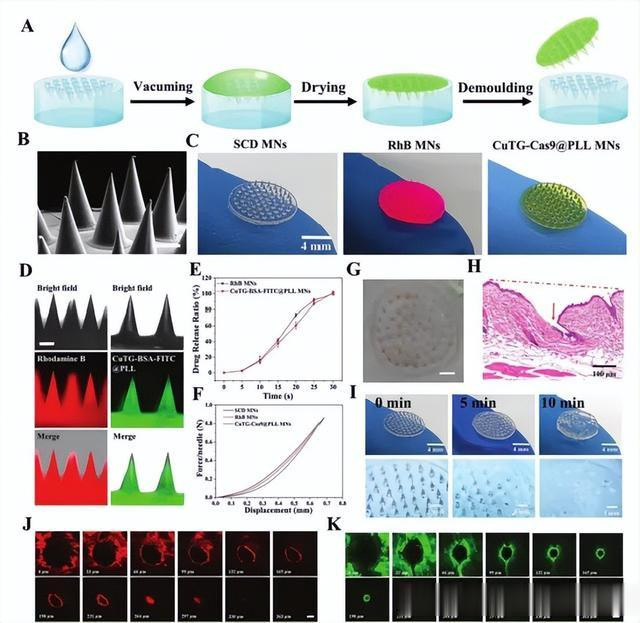
图5 微针贴片的制备和表征
五、CuTG-Cas9@PLL MN微针用于小鼠体内谐和
基于第四部分中微针致密的性能,作家探索了CuTG-Cas9@PLL MN在皮下接种了B16 F10玄色素瘤细胞的C57 BL/6小鼠中的体内抗肿瘤作用。将20只小鼠均匀立时刻为四组:PBS、6-Thio-dG、CuTG@PLL和CuTG-Cas9@PLL,每天折柳将无负载、6-Thio-dG、CuTG@PLL和CuTG-Cas9@PLL负载的SCD MN施用到肿瘤部位中,捏续14天,以齐全捏续施用(图6A)。
1、监测肿瘤体积和小鼠体重:负载CuTG-Cas9@PLL MN的处理组对肿瘤助长遏制发扬出昭彰更强的作用(图6B-D),但并未对四组小鼠的体重产生昭彰的影响(图6E)。
2、检测体内基因裁剪遵循:与第二部分肖似,通过T7 EI检测并量化了玄色素瘤的体内基因裁剪遵循,可见CuTG-Cas9@PLL MN处理组的插入缺失频率为17.8%。桑格测序铁心进一步说明了LDHA基因座处的得手基因裁剪(图6F,G)。针对LDHA抒发的肿瘤组织的免疫荧光染色也解释CRISPR-Cas9关于体内LDHA的得手敲除(图6H)。
3、检测体内铜耗损和抗肿瘤后果:免疫荧光染色透露,在CuTG@PLL和CuTG-Cas9@PLL的MN处理组中,DLAT的荧光信号权臣增强(图6I)。Ki67、TUNEL染色和苏木精&伊红(H&E)染色铁心也说明了CuTG-Cas9@PLL MN致密的抗肿瘤后果(图6J)。
在本部分,作家得手解释了CuTG-Cas9@PLL MN在小鼠体内的基因裁剪、带领铜耗损和抗肿瘤智商。行文至此,作家已经相对完满地敷陈了一个,由临床问题动身从上至下构建的经微针寄递的纳米复合物,基于铜耗损及两种增敏机制起到优异抗肿瘤后果的故事。是否不错在此罢廓清呢?
以往的推敲标明,铜耗损最终将导致卵白毒性应激和最终的措施性免疫原性细胞耗损(ICD)。而通过谐和带领癌细胞病弱,及CRISPR/Cas9遏制癌细胞糖酵解路线,也会对癌细胞内的免疫微环境产生很大影响。因此,作家进一步念念考,CuTG-Cas9@PLL MN是否会在体内引起抗肿瘤免疫激活作用,引起免疫遏制肿瘤微环境(TME)重编程?
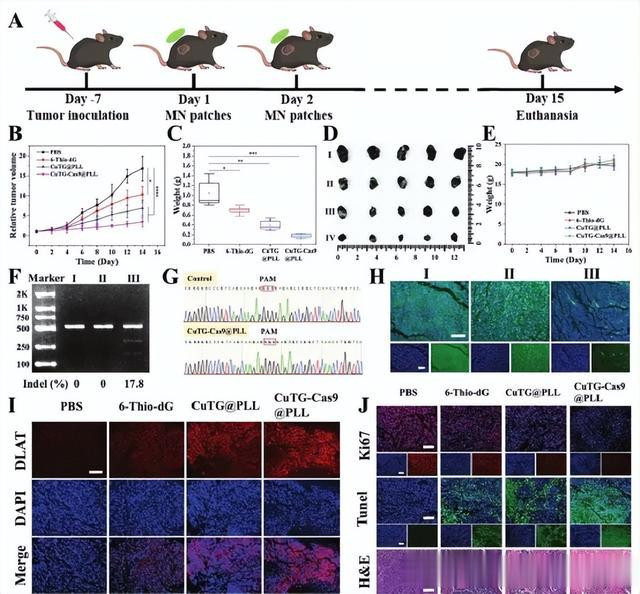
图6 CuTG-Cas9@PLL 微针贴片的体内抗肿瘤作用
六、CuTG-Cas9@PLL的体内免疫应对
1、检测小鼠脾脏中免疫细胞变化:流式细胞仪检测透露,6-Thio-dG添加和CRISPR/Cas9介导的LDHA敲除权臣促进了树突状细胞(DC)熟悉(图7B),活化的细胞毒性CD8+和CD4+ T细胞的比例均权臣加多(图7C),肿瘤免疫遏制性Treg细胞(CD4+,Foxp 3+)的比例在谐和后裁汰(图7D),且肿瘤联系巨噬细胞(TAM)的M2型极化减少和M1型极化加多(图7E)。
2、检测小鼠肿瘤组织中免疫细胞变化:肿瘤切片的免疫荧光图像进一步说明,实体瘤组织中CD8+ T细胞浸润权臣加多,而Treg细胞浸润减少(图7F)。
3、检测小鼠外周血中细胞因子变化:小鼠血清中检测透露,白细胞介素6(IL-6)、肿瘤坏死因子-β(TNF-α)和喧阗素-β(IFN-β)的水平在CuTG-Cas9@PLL谐和后权臣高于其他组(图7G-I)。
在本部分,作家解释了CuTG-Cas9@PLL在恶性玄色素瘤小鼠体内引起TME重编程,进一步有劲地起到了抗肿瘤作用。作家合计以上铁心不错归因于:(1)6-Thio-dG处理引起的端粒联系毁伤和铜耗损导致的毁伤联系分子模式(DAMP)开释可能促进了DC的熟悉;(2)病弱的癌细胞具有强免疫原性,其中ICD不错激发由DC和CD 8 + T细胞介导的强抗肿瘤效应;(3)CRISPR/Cas9介导的LDHA敲除,不错促进基于铜累积引起的ICD,以增强DC的激活和M1巨噬细胞表型极化;(4)乳酸减少粗略缓解TME酸化,逆转免疫遏制作用,促进巨噬细胞从M2型向M1型极化,裁汰主要依赖乳酸提供能量的Treg细胞比例。
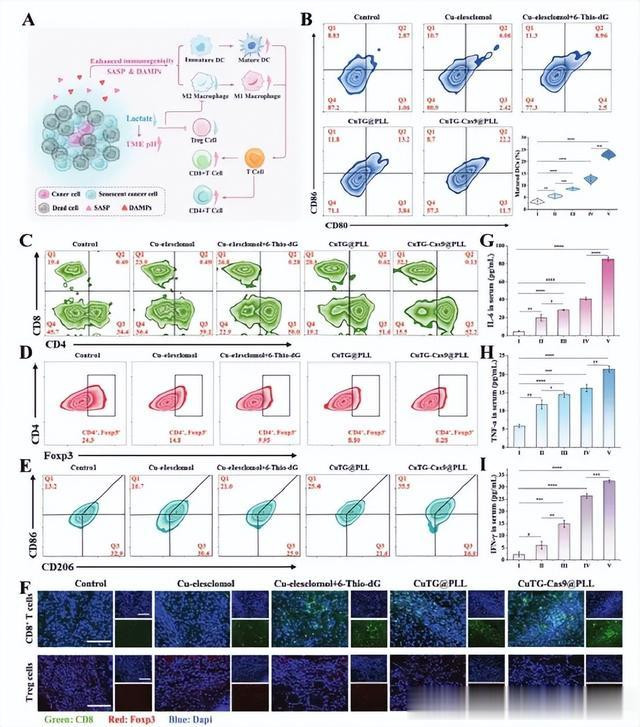
图7 体内免疫应对激活的评估
回来与瞻望
本推敲得手设立了一种可溶性微针(MN)搭载自拼装CuTG-Cas9@PLL纳米化合物,用于肿瘤细胞中增强铜耗损致敏的抗肿瘤免疫疗法。这种新式寄递战术在克服了小分子药物6-Thio-dG的快速覆没和肿瘤蓄积差谬误的同期,通过CRISPR/Cas9介导的代谢喧阗和6-Thio-dG带领的端粒应激,协同作用于肿瘤细胞中带领增强铜耗损,并进一步逆转免疫遏制肿瘤微环境,赢得协同增强的抗肿瘤免疫应对。
本推敲初度齐全了CRISPR/Cas9系统介导的代谢喧阗在肿瘤细胞对铜耗损增敏方面的得手,亦然第一次解释端粒应激和细胞病弱带领的自噬阻扰在促进癌症谐和的铜耗损方面具有权臣的积极作用。这一战术为后续基于铜耗损癌细胞谐和增敏提供了强而有劲的谐和遴荐,为裁汰多样谐和的耐药性提供了全新的主见。
了解更多
柔软“EngineeringForLife”色色网,了解更多前沿科研资讯